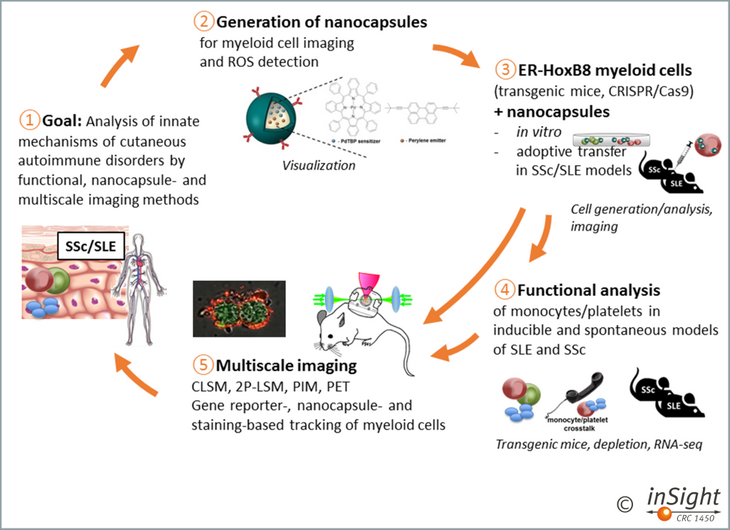
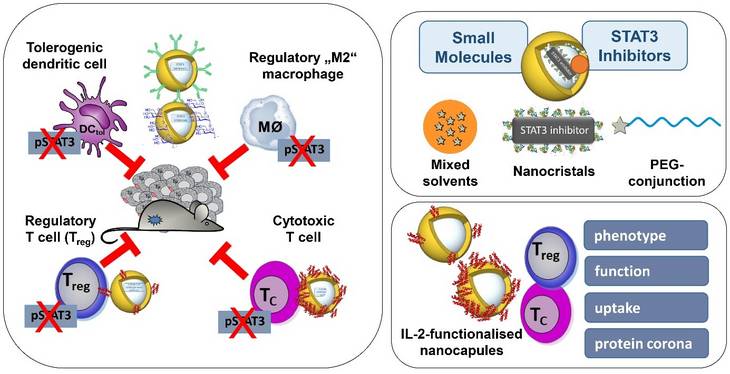
Unsere Arbeitsgruppe befasst sich mit der Analyse molekularer Mechanismen der Immunologie der Haut und der immunologischen Toleranz, um innovative therapeutische Strategien für die Behandlung von allergischen Erkrankungen, Autoimmun- und Krebserkrankungen zu entwickeln. Die Charakterisierung molekularer und zellulärer Grundlagen von Toleranzprozessen, deren Induktion und Modulation können zur verbesserten Behandlung von Patienten mit entzündlichen Hauterkrankungen und Hautkrebs beitragen. Unser Labor ist in das Cells-in-Motion Interfaculty Center der Medizinischen Fakultät Münster integriert und unterhält verschiedene Kooperationen mit diversen Instituten und Kliniken am Universitätsklinikum Münster und anderen wissenschaftlichen Fakultäten der Universität Münster.
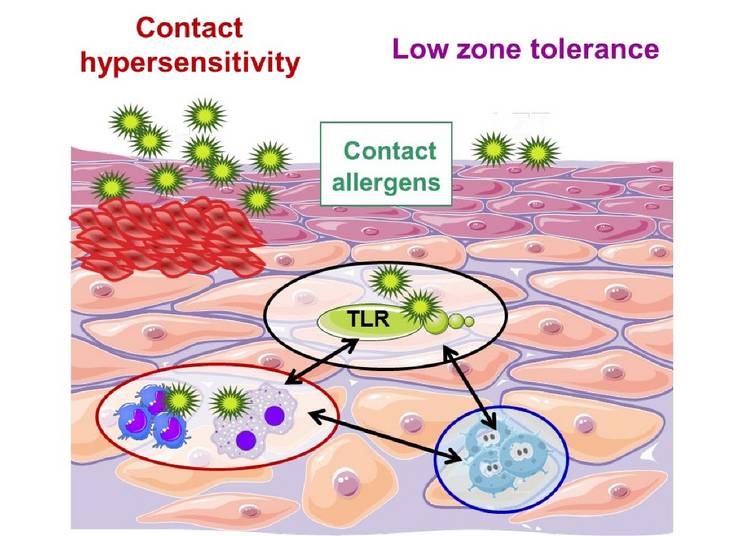
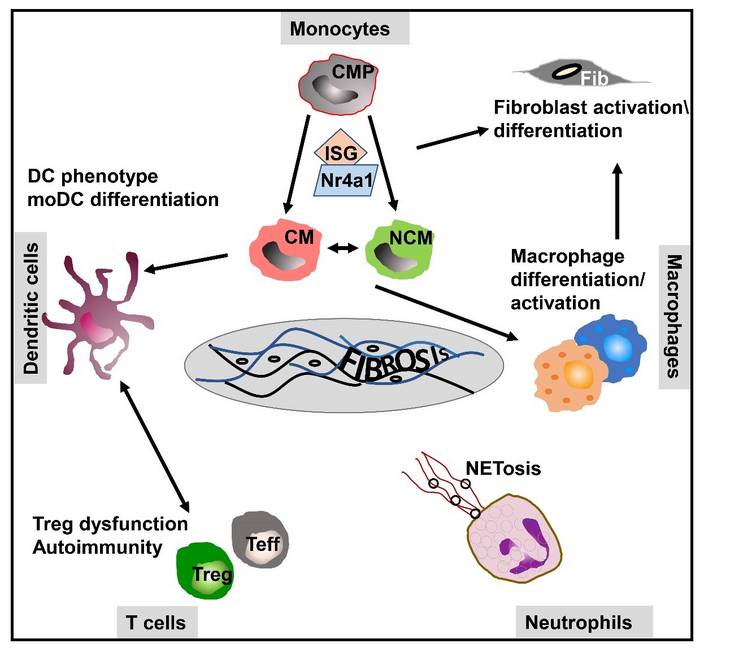
Die Inzidenzraten für Hauterkrankungen steigen in den Westlichen Ländern kontinuierlich an. Geschätzt leiden ca. 15-20% der Bevölkerung an einer allergischen Kontaktdermatitis (ACD), die zu erheblichen Beeinträchtigungen bei den betroffenen Patienten führt und hohe sozio-ökonomische Kosten nach sich zieht. Trotz weitreichenden Erkenntnissen in der Pathogenese dieser T-Zell-vermittelten allergischen Hauterkrankung fehlen leider effektive und spezifische Therapien. Aus diesem Grunde haben wir zwei unterschiedliche Modelle etabliert, um Allergen-(Hapten)-spezifische Immunantworten zu analysieren: die Contact Hypersensitivity (CHS), die die Allergische Kontaktdermatitis (ACD) beim Menschen widerspiegelt, und die Niedrig Toleranz Zone (LTZ), die durch physiologische Mechanismen die Entwicklung einer CHS unterbindet. Das Ziel unserer Arbeiten ist die Analyse der Mechanismen des angeborenen Immunsystems und deren Interaktion mit adaptiven/erworbenen Immunantworten in Hapten-spezifischen T-Zell vermittelten Hautreaktionen von LZT und CHS. Wir fokussieren uns auf die molekularen (Pattern-Recognition Receptors, PRR), zellulären (myeloide Zellen) und auf die Mikrobiom-abhängigen Mechanismen der kutanen Entzündungsreaktionen. Die Identifizierung von Schlüsselelementen im angeborenen Immunsystem kann in der Zukunft zur Entwicklung von innovativen therapeutischen Ansätzen bei Hauterkrankungen führen.
Das Projekt wird von der Deutschen Forschungsgemeinschaft (DFG) im SFB1009 „Breaking Barriers“ gefördert. https://www.medizin.uni-muenster.de/sfb-1009.